
セルバイオロジー
フェノタイプマイクロアレイ
遺伝子発現系分析システム
フェノタイプ(PM)システム

特長
約2000種のフェノタイプに対応する独自のPMパネルに微生物懸濁液を分注
所定の温度で培養しながらカイネティックをモニタリング
所定の温度で培養しながらカイネティックをモニタリング
A BREAKTHROUGH TECHNOLOGY
フェノタイプマイクロアレイ(PM)は研究や創薬(Figure 1)に関する遺伝子領域におけるDNAマイクロアレイ及びプロテオミクス技術に続く、第3のテクノロジーです。DNAマイクロアレイやプロテオミクス技術は一度に数千の遺伝子やタンパク質のレベル解析を可能にしてきました。フェノタイプマイクロアレイは一度に数千の細胞発現系の定量測定を可能にします。
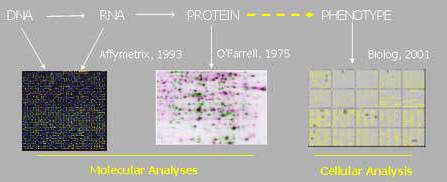
DNAマイクロアレイ及びプロテオミクス技術は、病状などと重要な相関性の変化パターンを調節する遺伝子やタンパク質の検出を可能にしました。しかしながら、これらの変化が細胞に対して顕著であるという保障はありませんでした。フェノタイプマイクロアレイは細胞などのレベルで必要とされる情報を提供する補完的な技術です。
フェノタイプマイクロアレイは、遺伝子機能の同定、薬剤ターゲットの評価、最適化や毒性研究の総合的な細胞プロファイルを提供します。遺伝子変化又はリード薬剤に対する暴露の後に、変化の細胞内応答を直接評価できます。
現在のところフェノタイプシステムは微生物及び菌類に対して使用できます。哺乳動物細胞用のプレートも開発中です。
フェノタイプマイクロアレイは、遺伝子機能の同定、薬剤ターゲットの評価、最適化や毒性研究の総合的な細胞プロファイルを提供します。遺伝子変化又はリード薬剤に対する暴露の後に、変化の細胞内応答を直接評価できます。
現在のところフェノタイプシステムは微生物及び菌類に対して使用できます。哺乳動物細胞用のプレートも開発中です。
HOW PM TECHNOLOGY WORKS
フェノタイプマイクロアレイは画期的なテクノロジーです。細胞のHTS用の装置やソフトウエアを統合した細胞アッセイシステムです。
テクノロジーとテストプロセスを下のFigure 2に示します。BioLog社はアレイセットにおける発現系テストの幅広い範囲を事前に構成します。アレイの各ウェルには異なった発現系に対するテストの培地がセットされています。前培養した標準細胞懸濁液をマイクロアレイの各ウェルに入れるだけで、様々なタイプの発現系のテストを1度に行うことが出来ます。マイクロアレイは通常24時間培養されます。
テクノロジーとテストプロセスを下のFigure 2に示します。BioLog社はアレイセットにおける発現系テストの幅広い範囲を事前に構成します。アレイの各ウェルには異なった発現系に対するテストの培地がセットされています。前培養した標準細胞懸濁液をマイクロアレイの各ウェルに入れるだけで、様々なタイプの発現系のテストを1度に行うことが出来ます。マイクロアレイは通常24時間培養されます。

フェノタイプマイクロアレイは、ユニバーサルなレポーターとして細胞の呼吸による、酸化還元化学を用いて評価(特許取得)します。ウェル内で強ポジティブな発現系があるならば、テトラゾリウム染料が還元され、強く発色(Figure 2左側)します。弱ポジティブ又はネガティブならば、固有は遅くなるか、停止し、発色が弱いか、発色しません。酸化還元反応により、発現系の頻度と精度の高い定量が可能になります。
培養及び発現系データの記録は、1時間に複数回マイクロアレイのデジタルイメージを撮影可能で、発色の変化を定量的にPCに保存するOmniLogシステムにより実行されます。データファイルはカイネティクスグラフの形式で表示されます。OmniLogシステムにより数千の発現系データ及び24時間の測定の間に記録される最大45万データポイントが同時にモニターされます。
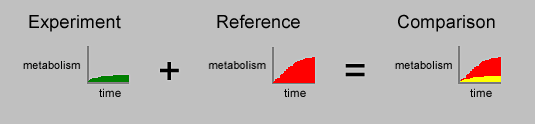
二つの細胞ラインの発現系を比較するために、片方は赤色のトレースとして、もう一方は緑色のトレースとして記録(Figure 2右側)されます。これらのグラフはバイオインフォマティックソフトウエアにより重ねあわされ、直接比較されます。重なっているエリア(変化無し)は黄色で表示され、差が表れているエリアは赤色又は緑色で表示(Figure 2右側及びFigure 3)されます。
培養及び発現系データの記録は、1時間に複数回マイクロアレイのデジタルイメージを撮影可能で、発色の変化を定量的にPCに保存するOmniLogシステムにより実行されます。データファイルはカイネティクスグラフの形式で表示されます。OmniLogシステムにより数千の発現系データ及び24時間の測定の間に記録される最大45万データポイントが同時にモニターされます。
二つの細胞ラインの発現系を比較するために、片方は赤色のトレースとして、もう一方は緑色のトレースとして記録(Figure 2右側)されます。これらのグラフはバイオインフォマティックソフトウエアにより重ねあわされ、直接比較されます。重なっているエリア(変化無し)は黄色で表示され、差が表れているエリアは赤色又は緑色で表示(Figure 2右側及びFigure 3)されます。
フェノタイプマイクロアレイは直接又は間接的に細胞の機能の既知アスペクトをモニターします。
フェノタイプの範囲には次の項目が含まれます。
・ 細胞表面構造及び輸送機能
・ 炭素、窒素、リン酸や硫黄の異化
・ 低分子の生合成
・ 高分子及び細胞器官の合成及び機能
・ 細胞呼吸機能
・ ストレス及び修復機能
・ その他の細胞機能
フェノタイプの範囲には次の項目が含まれます。
・ 細胞表面構造及び輸送機能
・ 炭素、窒素、リン酸や硫黄の異化
・ 低分子の生合成
・ 高分子及び細胞器官の合成及び機能
・ 細胞呼吸機能
・ ストレス及び修復機能
・ その他の細胞機能
Overview of Uses and Applications
PMテクノロジーの重要なアプリケーションは下に示すような3種類の主要なカテゴリーに分けられます。
I 細胞ラインへの薬剤や化学物質に対する暴露の研究
- 新規薬剤候補の評価
製薬及びバイオテクノロジー企業は薬剤候補のスクリーニングや評価に多くの時間や経費を費やしています。このプロセスは次の様な事象を迅速で精度の高いツールを用いることにより、効果的に且つ安価に評価できます。①薬剤の活動の場所やモード、②薬剤の作用と副作用、③その他の薬剤との相互作用など。PMテクノロジーは適正なツールを提供し、新薬の可能性評価の方法として使用できます。
実験のアプローチは形質変換した細胞をテストする非常にアナログ的なものです。ノックアウトなどの形質変換が起こっている場合、結果としていくつかの細胞機能がブロックされます。多くの薬剤は特定のタンパク質の機能をノックアウトすることをターゲットとします。このため、薬剤を添加した細胞は遺伝子をノックアウトしたものと、非常に似通った発現系の影響を受けます。
薬剤はPMシステムで培養されている間に添加されます。薬剤により変化のあった発現系を観察することにより、影響のあった細胞の生理学的機能を評価できます。この情報は次のように示されます。①薬剤活動の場所やモード、②薬剤がターゲットのどの部位にヒットしたか、又は、細胞内プロセスのどこに影響を与えたかとその結果による副作用、③その他の薬剤との相互作用。(多くの場合、PMテスト中の発現系は存在する薬剤に対する感度及び抵抗性が増強されます。)
- 毒性研究
細胞株の使用を基本とした毒性研究は動物実験からより安価なアプローチへと移り変わってきています。PMシステムを使用することにより、テストは薬剤開発の部分で記載した内容と本質的に同じ方法で行われます。細胞に化合物を添加し、PMシステムで培養します。細胞の生理学的影響がPMシステムで変化した反応により明らかになります。PMシステムからの情報は毒性のメカニズムと同様に毒性レベルとして評価されます。化合物の中には特定の成育条件や、その他の毒性化合物と作用して毒性を示すものがあります。PMシステムには数千の異なるテスト条件が含まれており、総合的な毒性情報を評価できます。
製薬及びバイオテクノロジー企業は薬剤候補のスクリーニングや評価に多くの時間や経費を費やしています。このプロセスは次の様な事象を迅速で精度の高いツールを用いることにより、効果的に且つ安価に評価できます。①薬剤の活動の場所やモード、②薬剤の作用と副作用、③その他の薬剤との相互作用など。PMテクノロジーは適正なツールを提供し、新薬の可能性評価の方法として使用できます。
実験のアプローチは形質変換した細胞をテストする非常にアナログ的なものです。ノックアウトなどの形質変換が起こっている場合、結果としていくつかの細胞機能がブロックされます。多くの薬剤は特定のタンパク質の機能をノックアウトすることをターゲットとします。このため、薬剤を添加した細胞は遺伝子をノックアウトしたものと、非常に似通った発現系の影響を受けます。
薬剤はPMシステムで培養されている間に添加されます。薬剤により変化のあった発現系を観察することにより、影響のあった細胞の生理学的機能を評価できます。この情報は次のように示されます。①薬剤活動の場所やモード、②薬剤がターゲットのどの部位にヒットしたか、又は、細胞内プロセスのどこに影響を与えたかとその結果による副作用、③その他の薬剤との相互作用。(多くの場合、PMテスト中の発現系は存在する薬剤に対する感度及び抵抗性が増強されます。)
- 毒性研究
細胞株の使用を基本とした毒性研究は動物実験からより安価なアプローチへと移り変わってきています。PMシステムを使用することにより、テストは薬剤開発の部分で記載した内容と本質的に同じ方法で行われます。細胞に化合物を添加し、PMシステムで培養します。細胞の生理学的影響がPMシステムで変化した反応により明らかになります。PMシステムからの情報は毒性のメカニズムと同様に毒性レベルとして評価されます。化合物の中には特定の成育条件や、その他の毒性化合物と作用して毒性を示すものがあります。PMシステムには数千の異なるテスト条件が含まれており、総合的な毒性情報を評価できます。
II 細胞ラインの遺伝子形質差の研究
- 重要な遺伝子の機能評価 (機能遺伝子)
細胞には2,000~120,000オーダーの遺伝子が含まれます。シンプルで多くの研究に用いられている微生物に関してでさえ、わかっている機能は半分程度です。遺伝子の多様性及び生化学手法を通して、研究者は特定の機能を同定しています。例えば、遺伝性ヒト遺伝学の研究ではこれらの遺伝子は重要な疾病や症候群に関連付けられています。その代わり、癌、微生物要因や慢性病に関連しており、新しい薬剤のターゲットとされています。生物学的及び商業的に重要性の高い遺伝子は、その他の動物、植物や微生物でも同定されています。しかしながら、現在のテクノロジーでは難易度が高く、効果であるだけでなく、重要な遺伝子機能の評価に対する直線的な方法ではありません。
未知遺伝子の機能を評価するための最も一般的な方法は、核酸ベースのマイクロアレイであり、信頼されています。DNAマイクロアレイは、複数の成育条件下でのmRNAレベルの測定に使用されており、データは未知遺伝子のmRNAレベルが既知遺伝子のmRNAレベルと相対的に増加又は減少することを観察することにより解析されます。望みは同一の方法で調節されるか、同じ機能経路のメンバーであると認めることが出来る遺伝子の遺伝子グループに依存します。このアプローチは時間がかかり、高価且つ複雑であり、非常に多くの仮定に基づいて実行されます。
PMシステムは細胞機能の興味のある遺伝子から直接たどり着くことを可能にします。実験のアプローチは系統のイソジェニックペアを作成する細胞株の遺伝子をノックアウトします。研究者はPMシステムでイソジェニック細胞株を培養し、数個のフェノタイプの違いを観察するだけです。細胞株に添加する遺伝子の遺伝子構造をノックインすることも出来ます。PMシステムで解析されたイソジェニック細胞株は、発現系の違いを一目で評価できます。イソジェニック系統の解析とPMシステムの使用により、ハイスループットの研究を遺伝子マップと、バーチャルの発現系マップの作成から開始できます。PMテクノロジーは遺伝子転写、翻訳や翻訳後変化などの仮定を含まない、迅速で安価であり、シンプルなシステムです。
- 新しい薬剤ターゲットをコードする遺伝子の検出
PMテクノロジーは新しい薬剤ターゲットを発見するための細胞株の比較に有用です。例えば、抗菌研究では病原及び非病原微生物の系統を比較できます。病原系統では薬剤体制遺伝子や病原アイランドなどの追加遺伝子が含まれていることが知られています。これらの遺伝子は、追加の発現系を病原菌に伝達するタンパク質をコードし、薬剤ターゲットとして有用です。
その他には新しい抗がん剤の研究にも使用されます。がん細胞を正常細胞と比較し、弱い部分の発現系を探索します。
- 細胞ラインの改質
多くの動物及び植物の遺伝子プロジェクトの主要な目的はターゲット細胞株又は種子の改良です。遺伝子操作後、細胞株は必要な発現系を獲得したか、また、不必要な発現系を獲得していないかを評価する必要があります。PMテクノロジーはこれらのタイプの開発に有用です。
- 細胞ラインの発現安定性のテスト
細胞株は経代培養を行うと変化する可能性があります。極僅かなこの部分は不安定な遺伝子構造と培養細胞に起こる未知の選択的圧力に依存します。細胞株の安定性は基礎研究にとって重要であり、ワクチンやリコンビナント蛋白の製造など、医療アプリケーションにとって特に重要です。細胞株の変化がいつ、どのようにして起こったのかを知ることが重要です。
細胞には2,000~120,000オーダーの遺伝子が含まれます。シンプルで多くの研究に用いられている微生物に関してでさえ、わかっている機能は半分程度です。遺伝子の多様性及び生化学手法を通して、研究者は特定の機能を同定しています。例えば、遺伝性ヒト遺伝学の研究ではこれらの遺伝子は重要な疾病や症候群に関連付けられています。その代わり、癌、微生物要因や慢性病に関連しており、新しい薬剤のターゲットとされています。生物学的及び商業的に重要性の高い遺伝子は、その他の動物、植物や微生物でも同定されています。しかしながら、現在のテクノロジーでは難易度が高く、効果であるだけでなく、重要な遺伝子機能の評価に対する直線的な方法ではありません。
未知遺伝子の機能を評価するための最も一般的な方法は、核酸ベースのマイクロアレイであり、信頼されています。DNAマイクロアレイは、複数の成育条件下でのmRNAレベルの測定に使用されており、データは未知遺伝子のmRNAレベルが既知遺伝子のmRNAレベルと相対的に増加又は減少することを観察することにより解析されます。望みは同一の方法で調節されるか、同じ機能経路のメンバーであると認めることが出来る遺伝子の遺伝子グループに依存します。このアプローチは時間がかかり、高価且つ複雑であり、非常に多くの仮定に基づいて実行されます。
PMシステムは細胞機能の興味のある遺伝子から直接たどり着くことを可能にします。実験のアプローチは系統のイソジェニックペアを作成する細胞株の遺伝子をノックアウトします。研究者はPMシステムでイソジェニック細胞株を培養し、数個のフェノタイプの違いを観察するだけです。細胞株に添加する遺伝子の遺伝子構造をノックインすることも出来ます。PMシステムで解析されたイソジェニック細胞株は、発現系の違いを一目で評価できます。イソジェニック系統の解析とPMシステムの使用により、ハイスループットの研究を遺伝子マップと、バーチャルの発現系マップの作成から開始できます。PMテクノロジーは遺伝子転写、翻訳や翻訳後変化などの仮定を含まない、迅速で安価であり、シンプルなシステムです。
- 新しい薬剤ターゲットをコードする遺伝子の検出
PMテクノロジーは新しい薬剤ターゲットを発見するための細胞株の比較に有用です。例えば、抗菌研究では病原及び非病原微生物の系統を比較できます。病原系統では薬剤体制遺伝子や病原アイランドなどの追加遺伝子が含まれていることが知られています。これらの遺伝子は、追加の発現系を病原菌に伝達するタンパク質をコードし、薬剤ターゲットとして有用です。
その他には新しい抗がん剤の研究にも使用されます。がん細胞を正常細胞と比較し、弱い部分の発現系を探索します。
- 細胞ラインの改質
多くの動物及び植物の遺伝子プロジェクトの主要な目的はターゲット細胞株又は種子の改良です。遺伝子操作後、細胞株は必要な発現系を獲得したか、また、不必要な発現系を獲得していないかを評価する必要があります。PMテクノロジーはこれらのタイプの開発に有用です。
- 細胞ラインの発現安定性のテスト
細胞株は経代培養を行うと変化する可能性があります。極僅かなこの部分は不安定な遺伝子構造と培養細胞に起こる未知の選択的圧力に依存します。細胞株の安定性は基礎研究にとって重要であり、ワクチンやリコンビナント蛋白の製造など、医療アプリケーションにとって特に重要です。細胞株の変化がいつ、どのようにして起こったのかを知ることが重要です。
III. 細胞ラインの直接テスト
- 培養細胞の最適増殖コンディションの評価
- 胞子形成及び培養の最適条件検索
- 抗体などの二次代謝物の最適生成条件検索
- 有用酵素活性の検出
- その他のセルベースアッセイ
- 胞子形成及び培養の最適条件検索
- 抗体などの二次代謝物の最適生成条件検索
- 有用酵素活性の検出
- その他のセルベースアッセイ
カタログはこちらダウンロードいただけます(PDF:2.39MB)
お問い合わせ
フォームが表示されるまでしばらくお待ち下さい。
恐れ入りますが、しばらくお待ちいただいてもフォームが表示されない場合は、こちらまでお問い合わせください。








